İçindekiler [gizle]
Atom Nedir ? Atom Modelleri Nelerdir ?
Bilinen evrenin en küçük yapı taşı atomdur. Antik çağlardan günümüze kadar gelen atomun hikayesi günümüzden çokta uzak olmayan zamanlarda neredeyse tam olarak çözüldü. Fakat hala kuantum fiziğinin tam olarak anlaşılamayışından veya tam olarak keşfedilemeyişinden kaynaklı olarak atom ölçeklerinde işlem yapmak pekte kolay değil.
Her atom bir çekirdekten ve çekirdeğin etrafına sarılmış bir veya daha fazla elektrondan oluşur. Bir atomun çekirdeği bir veya daha fazla proton ve nötrondan oluşur. Hidrojen atomlarının en yaygın biçimi dışında, tüm atom çekirdekleri nötron içerir. Elektronlar, proton ve nötronlara kıyasla o kadar küçüktür ki, tek başına proton ve nötronlar bir atomun toplam kütlesinin %99.94’ünü oluşturur.
Protonların pozitif elektrik yükü vardır. Elektronlar, negatif elektrik yüküne sahiptir. Nötronlarsa elektriksel olarak yüksüzdür. Eğer bir atomun çekirdeğindeki pozitif yüklü tanecik sayısı ile etrafındaki elektron sayısı birbirine eşitse, elektriksel olarak yüksüz olacaktır. Proton sayısı elektron sayısından fazlaysa o atom “pozitif”, elektron sayısı proton sayısından fazlaysa o atom “negatif” yüklü olacaktır. Bu şekilde pozitif veya negatif yüklü olan atomlara iyon denir.
Elektronlar, elektromanyetik kuvvet adı verilen bir kuvvet tarafından çekirdekteki protonlara çekilir. Protonları ve nötronları tek bir çekirdeğe bağlayan kuvvete güçlü nükleer kuvvet denir. Bu kuvvet ortalama olarak protonları iten elektromanyetik kuvvetten daha güçlüdür. Bu nedenle atomlar kolay kolay parçalanmazlar.
Ancak, belirli koşullar sağlandığında, bu elektromanyetik kuvvet, güçlü nükleer kuvveti yener ve atomlar bölünerek, yalnızca ana element dışındaki diğer elementlerin atomlarını bırakır. Bu bir tür nükleer dekompozisyondur(bozunmadır). Bir atomdaki proton sayısı, atom numarası adı verilen bir sayı ile temsil edilir. Ancak bir atomun proton sayısı aynı olsa bile nötron sayısı farklı olabilir. Bu tür atomlara izotop denir.
Atomlar, kimyasal bağlar adı verilen elektromanyetik etkileşimler yoluyla birbirlerine veya diğer atomlara bağlanabilir. Bu şekilde üretilen daha büyük birimler, moleküller ve kristaller gibi harfleri içerir. Evrende ve doğada gözlemlediğimiz tüm fiziksel ve kimyasal değişikliklerin temel nedeni atomların birbirine bağlanıp bu bağları gevşetebilme yeteneğidir.
Atomun doğasını inceleyen bilim dalı genellikle fizik iken, atomların değiş tokuşunu ve atomlar arasındaki etkileşimleri inceleyen bilim dalı kimyadır. Elbette fizik ve kimya sınırlarının çarpıştığı fiziksel kimya gibi alanlar da var.
Antik Çağda Atom
Antik çağlardan beri filozoflar maddenin en küçük yapı taşı hakkında kafa yormuş ve bu problemi çözmeye çalışmışlardır. En sonunda maddenin en küçük parçacığına, daha fazla bölünemez diye düşündükleri parçacığa Yunancada “atom-us” yani bölünemez adını vermişlerdir. Antik Yunan çağında yaşamış olan Leukippos ve onun öğrencisi Demokritos ve bunların ardılıları bu konu üzerinde kafa yormuş ve atoma bugünkü adını vermişlerdir. Özellikle Demokritos bu konu hakkında kendi dönemi içerisinde bilinenden çok daha ileriye giderek düşünsel çalışmalarda bulunmuştur
Atom Modelleri Nedir ?
Temel atom modelleri şunlardır;
- Democritos Atom Modeli
- Dalton Atom Modeli (Bilardo topu Atom Modeli)
- Thomson Atom Modeli(Üzümlü kek Atom Modeli)
- Rutherford Atom Modeli (Gezegensel Atom Modeli)
- Bohr Atom Modeli
- Modern Atom Modeli (Kuantum Atom Modeli)
Bu atom modellerini ve bunlara bulan, keşfeden, katkı sağlayan fizikçileri ufak bir yazı ile açıklamak gerekirse;
Democritos Atom Modeli
Democritos’a göre bir madde ayrıldığı zaman ortaya çıkan parçacık onun temel yapı taşıydı. Bu parça bölünemez ve görülemezdi. Democritos’a göre maddelerin farklı olmasının nedeni diziliş şekilleri ve atom sayısıydı. Bütün maddeler tek bir atomdan meydana geliyordu.
Evrenin ilk prensipleri atomlar ve boşluktur; diğer her şeyin sadece var olduğu düşünülür.
Democritos
Democritos’un hayatı ve görüşleri hakkında daha fazla bilgi almak için tıklayın.
Dalton Atom Modeli (Bilardo Topu Atom Modeli)

Günümüz atom modelinin temelini atmıştır. 1804 yılında “Katlı Oranlar Yasası”nı bulmuştur. Dalto’nun atom kuramına göre elementler, kimyasal bakımdan birbirinin aynı olan atomlar içerirler.
Dalton atom modeli 4 maddeye dayanır;
- Maddeler, atomlardan oluşur. Atomlar son derece küçük ve bölünemez parçacıklardır.
- Bir maddenin atomları aynıdır. Kütle, hacim veya boyut olarak bütün atomlar aynı özelliklere sahiptir. Diğer maddelerin atomları farklıdır.
- Bileşikler ise birden çok maddenin atomundan meydana gelir.
- Kimyasal tepkimeler atomların birbirinden ayrılması veya birleşmesi ile medyadan gelir.
Thomson Atom Modeli (Üzümlü Kek Atom Modeli)
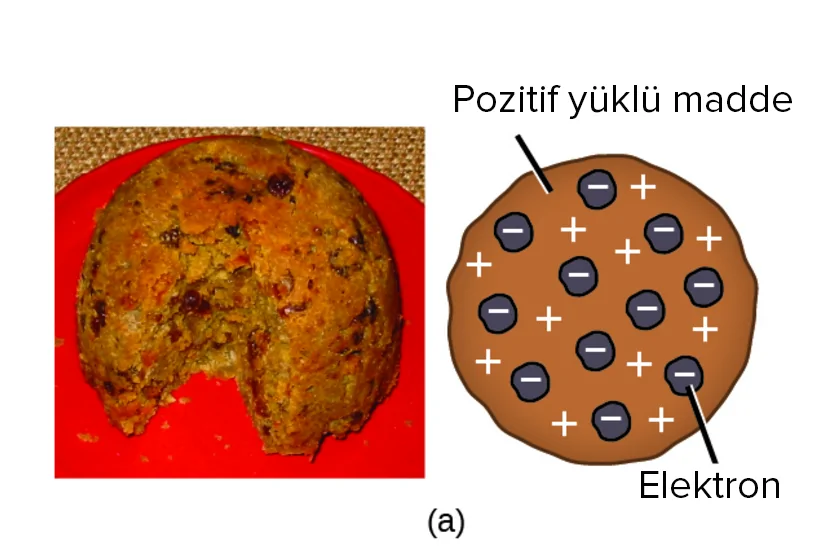
Thomson’a göre tıpkı bir üzümlü kek gibi atomların içerisinde pozitif yüklü elektronlar hem de negatif yüklü elektronlar vardır.
- Atomlar pozitif yüklü maddelerden oluşur.
- Bu pozitif maddedeki elektronlar hareketsizdir.
- Elektronların kütlesi çok küçüktür. Bir atomun toplam kütlesi, pozitif yüklü maddeden oluşur.
- Atomlar küreseldir.
Rutherford Atom Modeli (Gezegensel Atom Modeli)
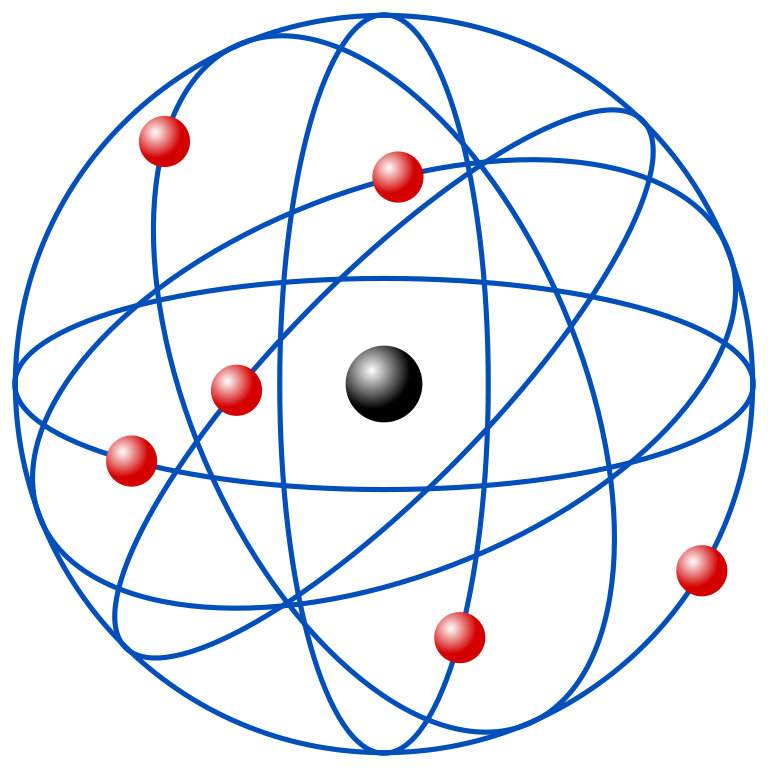
Modelin adından da anlaşılacağı üzere Rutherford atomu güneş sistemine benzetmiştir. Yaptığı deneyler sonucu elde ettiği verilere dayanarak atomun çoğunun bir boşluktan ibaret olduğunu, atom çekirdeğinin atom kütlesinin çoğunluğunu oluşturduğunu ve proton ile nötronların sayılarının aynı olduğunu gözlemlemiştir.
Niels Bohr Atom Modeli
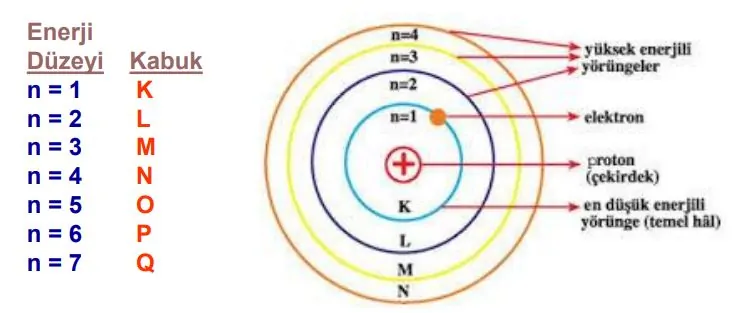
Bohr yaptığı deneyler ile elektronların çekirdekten uzakta tek bir yörünge de sabit olarak kalmadığını belirli yörüngelerde olduğunu gösterir. Bunu elektronların sahip olduğun enerji düzeyleri ile açıklar.
Atomlar söz konusu olduğunda, dil sadece şiirdeki gibi kullanılabilir.
Niels Henrik David Bohr
Modern Atom Modeli (Kuantum Atom Modeli)
Bütün bu fizikçiler ve bilim adamlarının çalışmalarının ardından artık günümüzde atomun gözlemlenebildiğini ve bölünebildiğini biliyoruz. Tüm bu çalışmalar sayesinde günümüzde artık Modern Atom Modeli kullanılmakta. Modern atom modeline göre elektronların hızının ve konumunun aynı anda bulunamayacağı ve elektronların belli yörüngesel hareketlerde bulunduğu bugüne kadar çalışmalarda bulunmuş ve hala bu konuda çalışmalarda bulunan atomu daha iyi anlamamızı sağlayan tüm bilim adamları tarafından kabul edilmiş ortak görüştür.
Modern atom modeli, Bohr modelinin neredeyse bir üst versiyonu gibidir. Onun açıklarını ve hatalarını kapatarak yeni bir atom modeli ortaya atılmıştır.








